
官方微信
2020 官網(wǎng)升級中!現(xiàn)在您訪問官網(wǎng)的瀏覽器設備分辨率寬度低于1280px請使用高分辨率寬度訪問。
 ENGLISH
ENGLISH
 400-0755-878
400-0755-878
為何選擇3D打印
3D打印制造技術在醫(yī)療健康領域的優(yōu)勢主要體現(xiàn)在以下幾個方面[1]。
材料及應用
醫(yī)療器械需滿足一定的尺寸精度、機械性能、生物兼容性(國際標準ISO-10993)、耐腐蝕。如下圖所示,醫(yī)用植入物可用于顱骨、下頜骨、肩胛骨、胸骨、脊柱、髖骨、膝關節(jié)和截骨相關的手術。用于3D打印的金屬材料主要為鈦和鈦合金,鉭,醫(yī)用不銹鋼,采用粉床激光或電子束選區(qū)熔覆工藝[2]。
從復雜的面部整形手術到骨科和創(chuàng)傷外科手術,例如顱骨的修復、下顎骨的整形,植入物的幾何形狀通常非常復雜。在患者安全和滿意度、醫(yī)院效率和經(jīng)濟效益方面,3D打印的植入物可以提供更好、更可預測的結果,比如提高手術成功率,降低需二次手術的可能性。
脊柱植入物被用來恢復患者的椎間高度。這類醫(yī)療器械通過輕量化的晶格結構設計來模仿骨骼機械特性,這里特指部件的彈性模量。傳統(tǒng)的制造技術無法生產(chǎn)出具有晶格結構的脊柱植入物,而晶格結構具有較高的表面積,可促進成骨細胞向植入物遷移,并能優(yōu)化多孔體的機械性能,以滿足所需的加載條件。
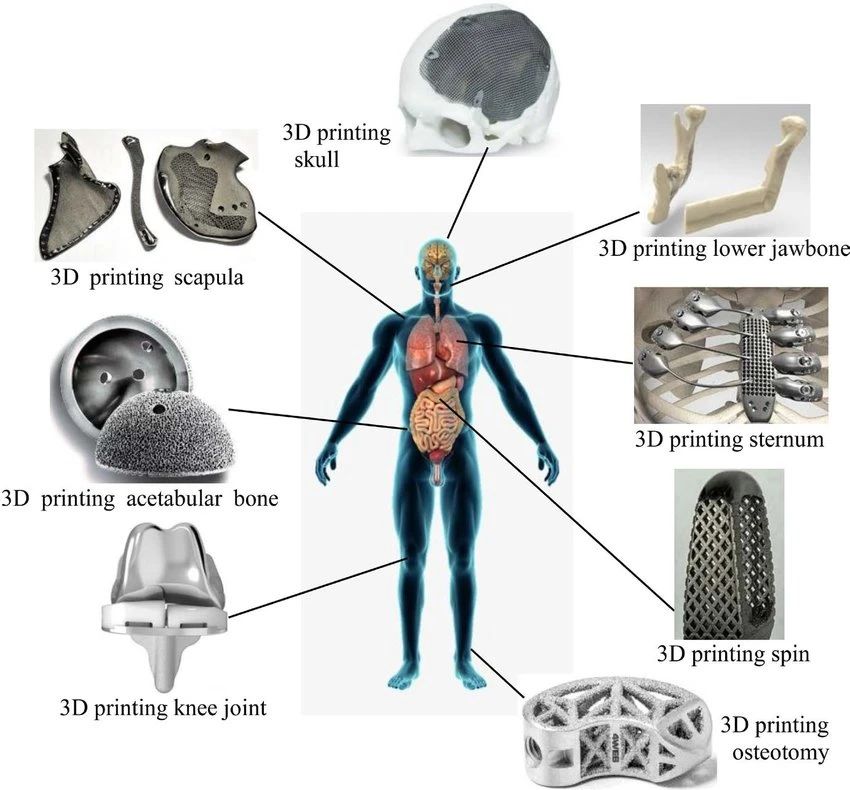
3D打印顱骨、下頜骨、肩胛骨、胸骨、脊柱、髖骨、膝關節(jié)、截骨。圖源:[3]

圖源:雷尼紹
工藝流程
通過結合X射線掃描、CT、核磁共振成像或超聲波掃描等技術獲得生物結構的醫(yī)學影像,3D打印技術可為每一位病例制造專用的植入物,其解剖結構幾乎與受傷組織相同。
針對3D打印植入物的常見后處理工藝有除粉,應力消除熱處理,去支撐,噴砂,磨料流拋光以及用來去除經(jīng)噴砂和磨流拋光后留在表面的碎片以及因部分熔化而粘結在表面的粉末顆粒的電解拋光[4]。在拋光過程中,通常會使用一些強腐蝕性的溶劑,比如用于外科植入式不銹鋼裝置的磷酸和硫酸混合液(ASTM A380)。最后,用去離子水清洗部件,干燥。
在某些應用中,表面改性的技術比如微弧氧化和表面涂層也被運用到3D打印的支架上。熱處理可以改善部件的表面粗糙度,有助于礦物質的富集,細胞的附著和生長。
標準與認證
盡管已經(jīng)有許多臨床試驗使用定制化植入物,然而,由于缺乏相關法規(guī)或法律的指導,3D打印在醫(yī)療植入物領域的發(fā)展可能會受到阻礙。
首先,醫(yī)療器械的生產(chǎn)需要滿足質量管理體系的認證要求,比如針對定制化植入物的國際標準ISO13485。在銷售或分銷前,制造商必須向目標市場所在的國家或地區(qū)注冊意向銷售的醫(yī)療器械,如中國的NMPA,歐盟的MDR以及美國的FDA。這些機構為制造商提供建議,其中包括3D打印醫(yī)療設備開發(fā)過程中的設備設計、制造和測試注意事項等。為了確保產(chǎn)品的性能,制造或者服務的可重復性以及可追溯性,地區(qū)機構會對制造商內(nèi)部建立的質量管理體系進行審核。
因為3D打印的整個工作流程始于從醫(yī)學影像到數(shù)字模型和加工文件的建立,瑪瑞斯率先對其設計軟件產(chǎn)品和切片等流程進行了認證,確保加工文件和實際生物結構相一致。為了確保.stl文件和構建文件中部件幾何尺寸的精度(具體工作流程如下圖所示),瑪瑞斯建立了可靠的數(shù)據(jù)庫。
此外,瑪瑞斯的團隊會定期通過文獻調(diào)研來了解用戶如何運用軟件開展不同的研究,并從中來找到軟件中影響切片準確性的弱點。瑪瑞斯在全球擁有廣大的客戶群體,可以更有效地對軟件實現(xiàn)迭代升級,提高其穩(wěn)定性。

切片軟件的驗證流程以及醫(yī)學影像(左),數(shù)字模型(中)和兩者尺寸差(右)的對比,圖源:瑪瑞斯

官方微信